

這是我見過的WB結果圖最多的文章!【文獻解讀】
 2020-12-17 15:53:24
2020-12-17 15:53:24
來源/作者:普拉特澤生物-醫學整體課題外包

這篇發表于Nat Commun( IF:11.8780)雜志上的文章將WB實驗從頭貫徹到尾,研究黑色素瘤細胞中ITCH/BRAF/MEK/ERK通路。
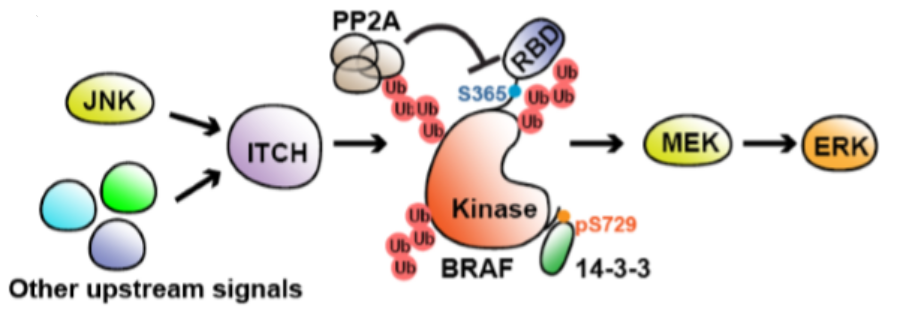
本文結論:在黑色素瘤細胞中,受到細胞因子的刺激,BRAF主要通過K27位點被多聚泛素化,且不導致最終的蛋白降解。這種非典型的泛素化作用是由ITCH E3連接酶響應c-Jun-N-末端激酶(JNK)介導的磷酸化作用而催化的。K27位點的BRAF泛素化消除了14–3–3介導的BRAF激酶活性抑制,導致BRAF / MEK / ERK信號得以維持,進而有助于腫瘤細胞因子促進黑色素瘤細胞的存活。
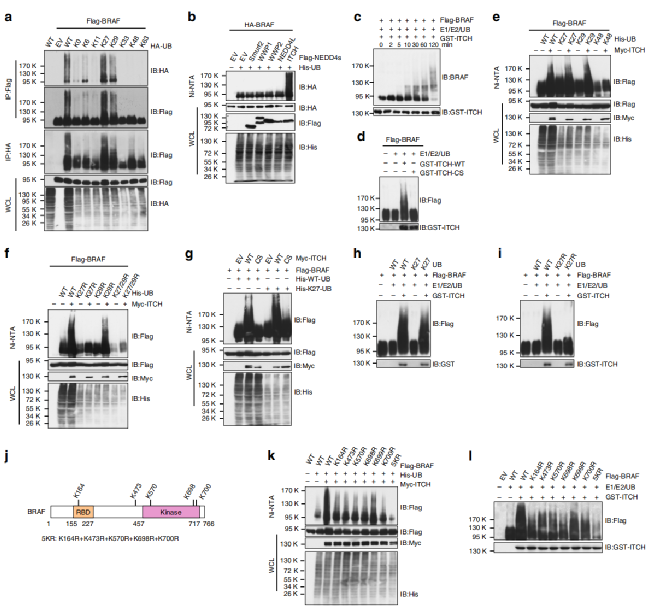
Fig 1. ITCH通過K27位點使BRAF泛素化
黑色素瘤細胞中,內源性BRAF的多泛素化。為了確定BRAF蛋白上的多聚泛素化位點,作者構建了BRAF單泛素化位點突變體,結果顯示,在K27位點存在的情況下泛素化水平最高(a)。之后用多種K27位點相關泛素化連接酶處理,其中ITCH顯著增強了BRAF的泛素化水平(b)。那么ITCH是否是通過K27位點對BRAF位點進行泛素化的呢?共轉染結果顯示K27、K29位點存在的情況下,BRAF的泛素化水平均顯著增加(e)。將K27、K29位點分別突變,發現K29位點突變后不影響ITCH的效果,綜上結果表明ITCH是通過K27位點對BRAF位點進行泛素化(f-i)。
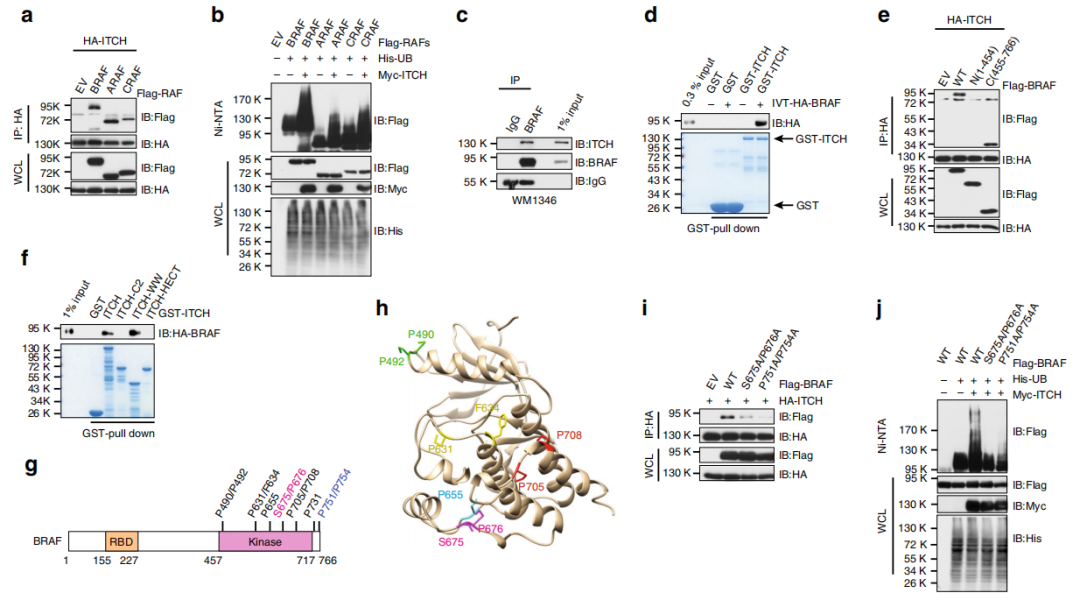
Fig 2. ITCH通過激酶結構域與BRAF相互作用
之后作者將重點放在闡明ITCH引起的BRAF泛素化如何決定黑色素瘤環境中的BRAF / MEK / ERK信號級聯。GST pull down實驗進一步證明了ITCH與BRAF直接互作(d)。作者發現BRAF的C末端激酶結構域直接與ITCH結合(e),ITCH利用其WW 結構域與BRAF互作(f)。在BRAF的激酶結構域中鑒定出許多非PPxY脯氨酸豐富的基序(g,h)。BRAF蛋白上S675/P676 或者P751/P754位點突變均可導致其與ITCH結合減少。總結以上結果,在BRAF激酶結構域中查明了兩個富含脯氨酸的基序,這些基序介導了ITCH-BRAF相互作用,以促進BRAF的K27位點多泛素化。
備注:
1.NEDD4家族泛素E3連接酶(包括ITCH)通過其WW結構域與其底物相互作用。
2.除了PPxY基序,NEDD4家族E3連接酶還通過其他富含脯氨酸的基序(例如PPLP,pSP或pTP基序)募集底物。
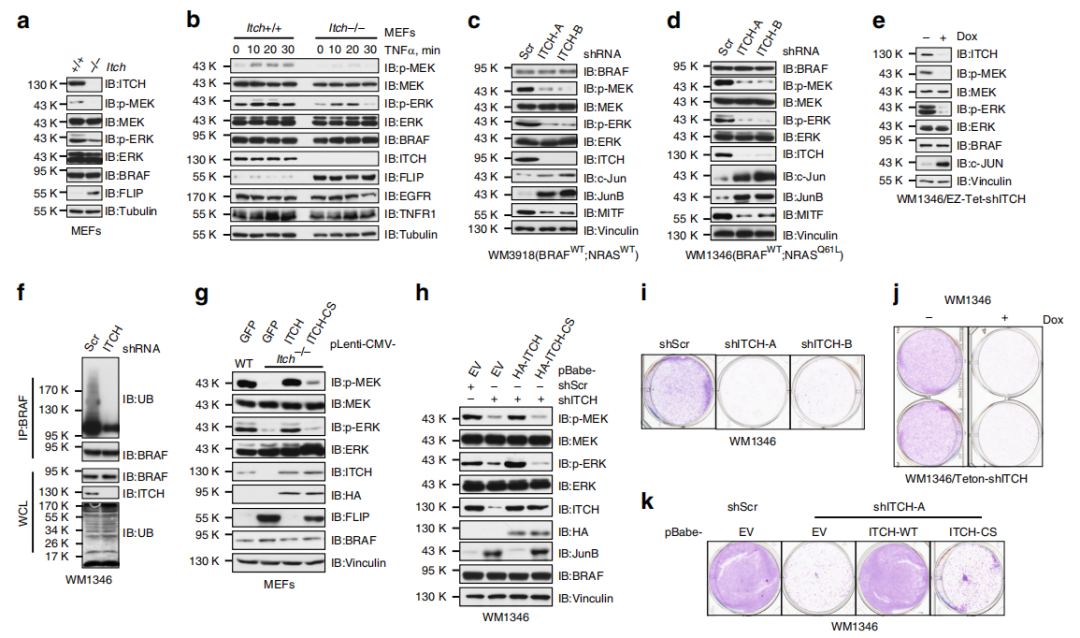
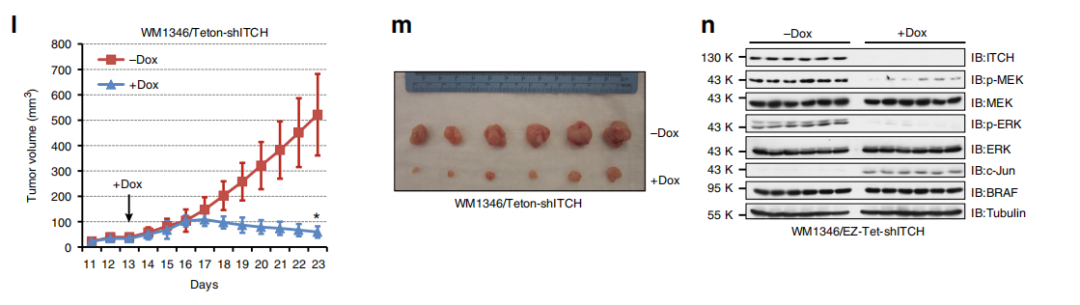
Fig 3. ITCH耗竭會減弱MEK / ERK信號傳導和細胞生長。
作者接下來通過構建Itch缺失突變體株來研究ITCH是否是MEK / ERK信號級聯反應的重要上游調節劑。與MEFs WT相比,Itch缺失的MEFs表現出降低的MEK / ERK活性(a),表明ITCH對BRAF功能的正調節作用。TNFα使得MEFs WT細胞中MEK / ERK信號快速激活,但是Itch缺失的MEFs細胞則對TNFα的刺激不敏感(b),在其他黑色素瘤細胞中也有同樣的實驗結果(d-e)。提示細胞因子誘導的MEK/ERK激活至少部分是通過ITCH途徑的,且調節MEK / ERK信號轉導依賴E3-連接酶活性(f-h)。
另外,作者發現ITCH敲降抑制細胞增殖(i,j),ITCH耗竭顯著抑制了p-MEK / p-ERK信號轉導和體內腫瘤生長。綜上表明,ITCH可以積極調節BRAF / MEK / ERK信號級聯,并促進BRAF WT黑色素瘤細胞的存活。
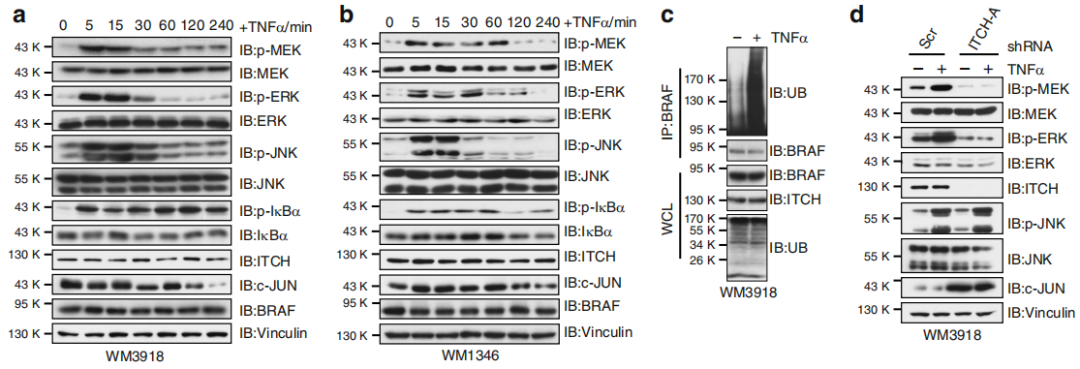
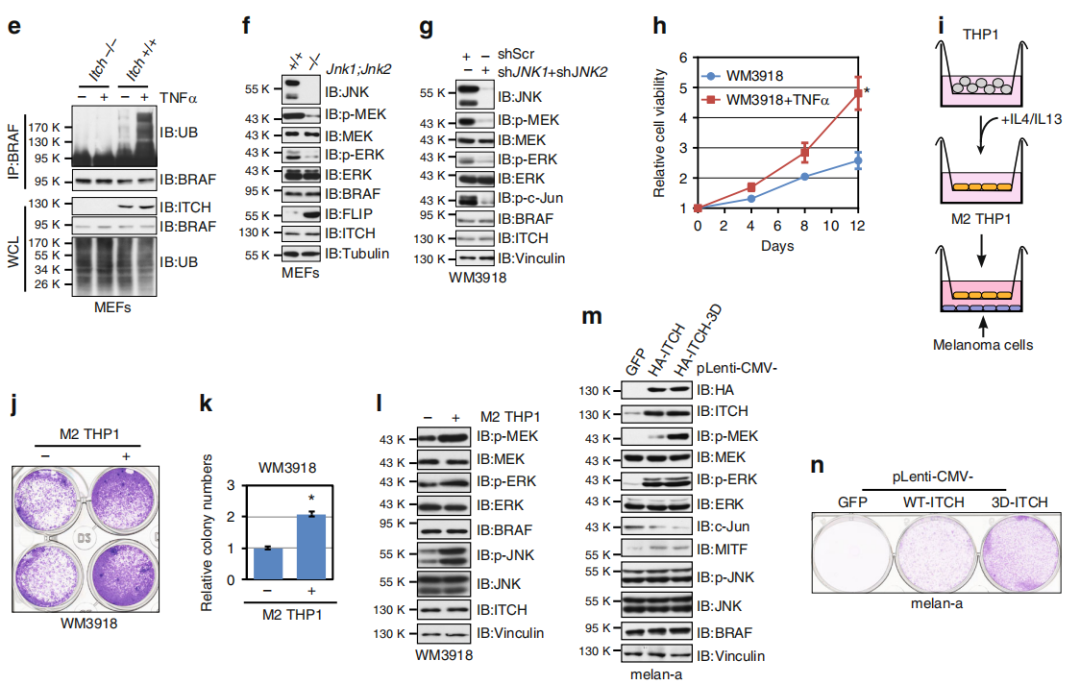
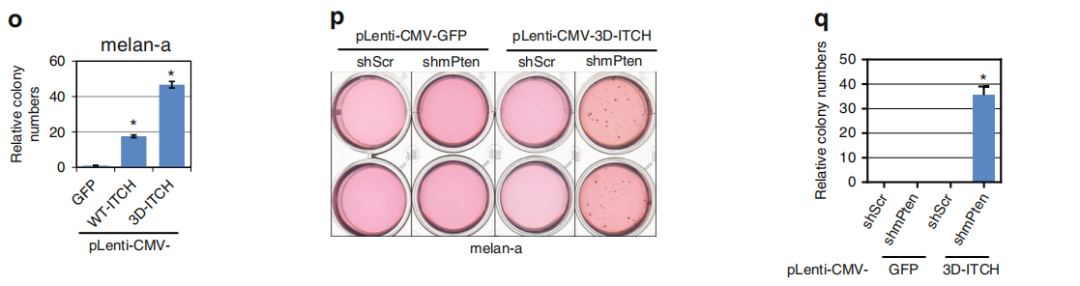
Fig 4. 細胞因子促進BRAF泛素化和激活
TNFα處理后誘導快速增加p-MEK/p-ERK水平,同時JNK水平上升(a,b),表明BRAF功能與 JNK/ITCH途徑激活具有相關性。在黑色素細胞和黑色素瘤細胞中,TNFα處理后BRAF 泛素化增加(c),而ITCH耗竭的黑色素瘤細胞中p-MEK/p-ERK對TNFα治療無效(d)。MEF中的Itch缺失可消除TNFα介導的BRAF泛素化(e)。MEF中Jnk1和Jnk2的缺失導致ITCH失活的同時導致p-MEK和p-ERK的水平降低(f)。此外,在黑色素瘤細胞中敲低JNK1和JNK2抑制了MEK和ERK活性(g)。與對照細胞相比,用TNFα或IL-1β處理的黑素瘤細胞顯示出細胞生長增加(h)。腫瘤環境中促炎細胞因子的主要來源之一是腫瘤相關的巨噬細胞,特別是M2巨噬細胞。通過黑色素瘤細胞和M2巨噬細胞共培養(i),作者發現M2型的THP1細胞可以促進WM3918細胞的增殖(j,k),與對照細胞相比,在與M2型的THP1細胞共培養的細胞中觀察到p-JNK,p-MEK和p-ERK水平升高(l)。
總結,細胞因子刺激激活JNK并促進ITCH激活進而促進BRAF泛素化和隨后MEK / ERK信號升高。
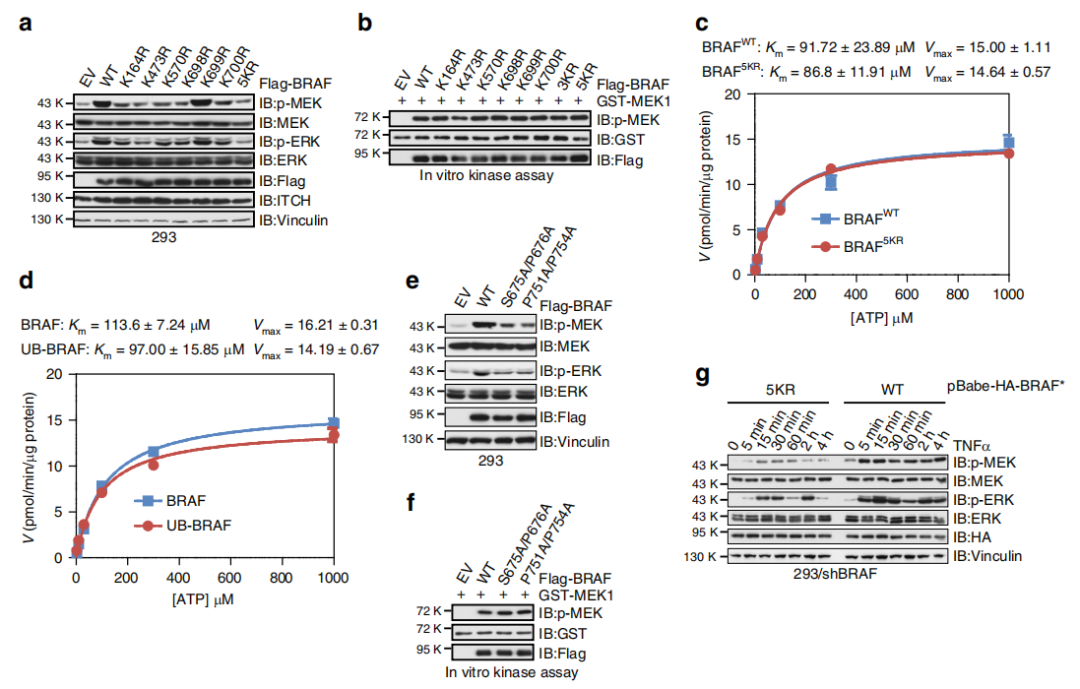
Fig 5. 泛素化缺乏的BRAF無法激活MEK / ERK
那么,BRAF的泛素化是否是下游因子激活的關鍵因子呢?與BRAFWT相比,除K699R外,所有KR突變體均表現低MEK / ERK活性(a)。BRAFKR突變體與BRAFWT表現出相似的磷酸化MEK1的活性(b)。此外,BRAFWT/BRAFKR在促進GST-MEK1磷酸化方面表現出相同的激酶動力學(c,d),表明KR突變幾乎不影響BRAF蛋白的構象。缺乏ITCH結合缺陷的BRAF S675A / P676A和P751A / P754A突變體在促進細胞中MEK / ERK信號轉導方面表現出降低的活性(e)。與表達BRAFWT的細胞相比,在表達BRAF5KR的細胞中,TNFα刺激極少觸發p-MEK和p-ERK的活化(g)。以上證明,泛素化缺陷型BRAF5KR的細胞對細胞因子刺激無效。
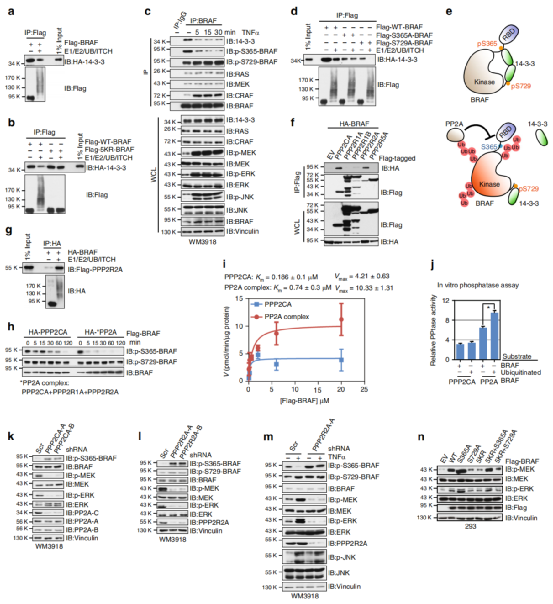
Fig6. 泛素化消除了BRAF / 14-3-3結合的抑制作用
與未修飾的BRAF相比,泛素化的BRAF與14-3-3的相互作用降低(a)。但是14-3-3與5KR-BRAF或ITCH結合區缺乏的BRAF的結合不受影響(b)。TNFα處理黑色素瘤細胞后,內源性BRAF與14-3-3蛋白的結合被減弱(c)。14-3-3二聚體介導的p-S365和p-S729位點的分子內相互作用使BRAF處于封閉的非活性構象,兩個BRAF蛋白的分子通過p-S729位點與14-3-3二聚體結合而變得更加穩定,作者發現S365或S729的突變導致與14-3-3的結合減少,泛素化以及未泛素化的S365A-BRAF與14-3-3結合無顯著差異(d)。因此,該結果證明K27位點的多聚泛素特異性干擾14-3-3與p-S365之間的結合(e)。
由于14-3-3與C末端p-S729位點的結合可促進RAF蛋白二聚化。
我們接下來試圖確定BRAF多泛素化是否控制BRAF二聚化。作者假設K27連接的聚泛素鏈可能募集PP2A磷酸酶去磷酸化p-S365,從而導致與細胞中14-3-3的結合進一步減少(e),從而維持BRAF 驅動下游MEK / ERK信號的活動。作者發現,與未修飾的BRAF相比,泛素化的BRAF與PPP2R2A亞基具有更強的結合力(g)。為了支持PP2A在調節BRAF活性中的關鍵作用,作者發現在黑色素瘤細胞中,PPP2CA或PPP2R2A的耗竭導致p-S365-BRAF升高,MEK / ERK活性降低(k,1)。綜上說明了BRAF K27位點的泛素化在破壞14-3-3介導的BRAF抑制中的獨特作用。
備注:BRAF的上游調節子。14–3–3蛋白識別RSxpSxP或RxxxpSxP基序,其中pS代表磷酸絲氨酸。p-S365,而p-S729是在BRAF中發現的14–3–3相互作用位點。
PP2A家族:PPP2CA亞基和B55亞家族調節性亞基PPP2R2A與BRAF具有很強的結合力。PP2A全酶由三個亞基組成:支架亞基A,催化亞基C和四個調節亞基B。
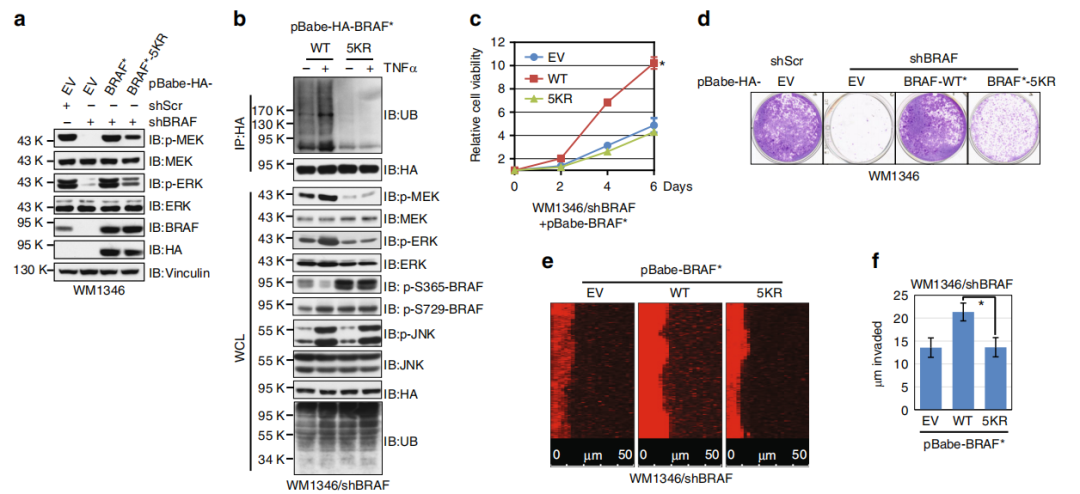
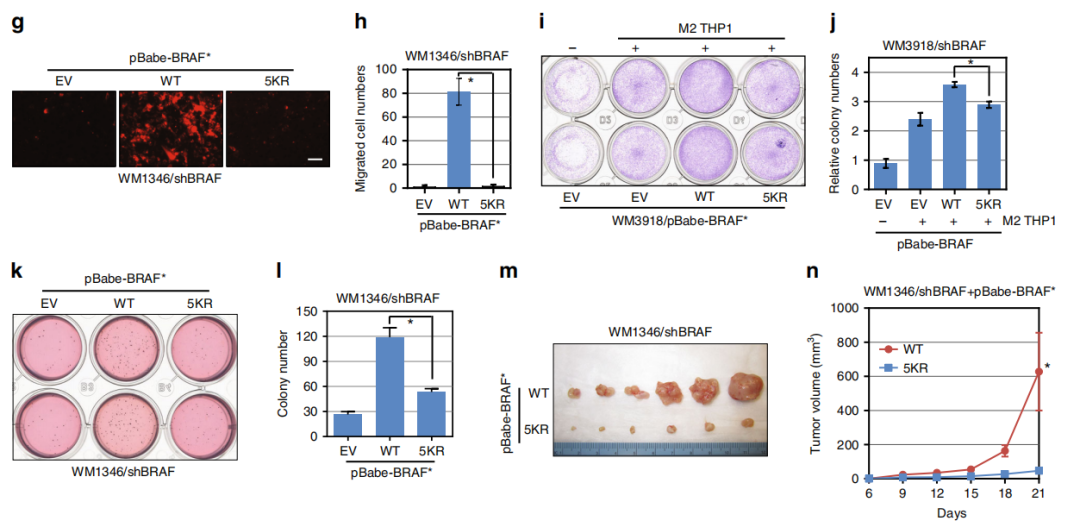
Fig7. 泛素缺乏的BRAF致瘤性較低
那是否泛素缺乏的BRAF突變體在BRAFWT的黑色素瘤細胞的生長和侵襲中表現出功能受損。作者發現與BRAFWT相比,泛素化缺乏的BRAF5KR無法促進BRAF缺失的黑色素瘤細胞中MEK / ERK的活化(a),且表達BRAF5KR的WM1346細胞對TNFα介導的MEK / ERK活化具有抵抗力,并伴隨泛素化降低(b)。在BRAF敲除的細胞系中重建BRAFWT后發現細胞增殖被促進,而BRAF 5KR重建組則表現細胞增殖活性的降低(c,d)。表明K27位點的多泛素化在維持黑素瘤細胞中BRAF活性中起著至關重要的作用。
此外,表達BRAF5KR的細胞表現出低的基質膠(e,f)內皮細胞(g,h)的侵襲能力。M2分化的THP1細胞刺激了BRAFWT WM3918細胞的生長,但在BRAF5KR的細胞中卻沒有這種作用(i,j)。
BRAFWT的表達促進了免疫缺陷小鼠的腫瘤生長,但帶有BRAF5KR的WM1346細胞體內致瘤性較小(m,n)。
綜上,與BRAFWT相比(促進黑素瘤細胞的增殖和侵襲),泛素化不足的BRAF5KR突變體活性較低,且表現出受損的致癌功能,這些數據支持非典型泛素化BRAF的翻譯后修飾,以維持黑色素瘤細胞中MEK / ERK信號轉導的級聯。
