

Crispr/Cas9基因編輯介紹
 2025-01-16 16:23:45
2025-01-16 16:23:45
來源/作者:普拉特澤-生物醫學整體課題外包平臺
CRISPR/Cas9技術是區別于ZFN與TALENs的最新基因編輯技術,并在近年迅速得到推廣與應用。該技術擁有修飾效率高、操作簡便、成本廉價等多個優點,因此在目前各項生物研究中成為最主流的基因編輯方式。
(一)技術起源與發展
CRISPR-Cas 系統最初是在細菌和古細菌的免疫系統中被發現的,它能夠幫助這些微生物識別和抵御外源遺傳物質的入侵,如噬菌體病毒和外源質粒等。
2012 年,科學家詹妮弗?杜德納(Jennifer Doudna)和艾曼紐?夏彭蒂耶(Emmanuelle Charpentier)首次證明了 CRISPR-Cas9 系統在體外可以對 DNA 進行特異性切割。
2013 年,張峰等人將 CRISPR-Cas9 技術成功應用于哺乳動物細胞的基因編輯,開啟了該技術在生物醫學領域廣泛應用的大門。
(二)系統組成與結構
Cas9 蛋白:是一種核酸內切酶,具有切割雙鏈 DNA 的功能。它包含 RuvC1 和 HNH 樣核酸酶結構域,這兩個結構域分別負責切割 DNA 的兩條鏈,從而產生雙鏈斷裂。Cas9 蛋白行使功能需要依賴向導 RNA 的引導以及靶序列相鄰的原型間隔序列毗鄰基序(PAM)的識別。
向導 RNA(gRNA):由 CRISPR 轉錄產生的 crRNA 與反式激活的 tracrRNA 融合而成的單鏈引導 RNA(sgRNA)。sgRNA 的 5′端包含與靶 DNA 互補的 20nt 左右的序列,用于定位需編輯的位點;3′端則是與 Cas9 蛋白結合的區域,通過與 Cas9 蛋白相互作用,引導其到達目標基因的特定 DNA 序列上。
(三)作用機
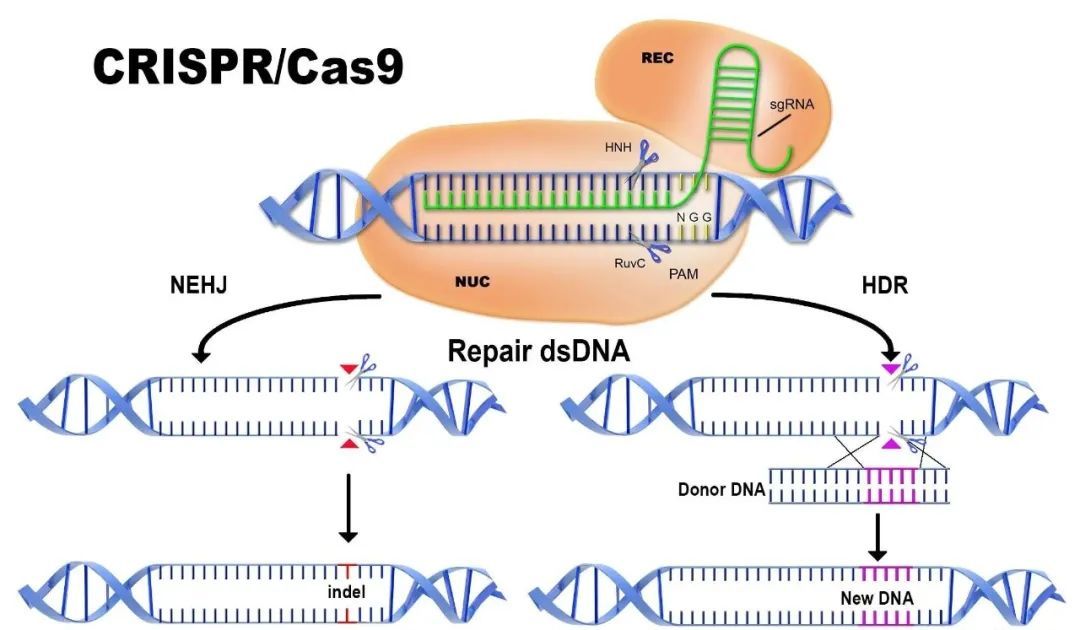
識別與結合:sgRNA 首先與 Cas9 蛋白形成復合物,然后通過其 5′端的互補序列在基因組中尋找與之匹配的靶 DNA 序列。當找到匹配的靶序列后,sgRNA-Cas9 復合物會與靶 DNA 結合,同時識別靶序列下游的 PAM 序列,PAM 序列一般為 5′-NGG,它作為一種識別信號,確保 Cas9 蛋白能夠準確地結合到目標 DNA 上。
切割作用:在結合到靶 DNA 后,Cas9 蛋白的核酸酶結構域會被激活,分別在 PAM 序列上游第 3 個堿基處對 DNA 的兩條鏈進行切割,產生雙鏈斷裂。這種雙鏈斷裂是細胞內 DNA 修復機制啟動的信號,細胞會通過非同源末端連接或同源重組修復機制來修復斷裂的 DNA。

修復與編輯:非同源末端連接是一種易錯的修復方式,在修復過程中常常會引入插入或缺失突變,導致基因閱讀框發生改變,從而使基因功能喪失,實現基因敲除的效果。而如果在細胞中同時提供含有目的基因片段的供體 DNA 模板,細胞則會通過同源重組修復機制,以供體 DNA 為模板,將目的基因片段精準地插入到靶位點,實現基因敲入或替換等精確編輯。
(四)CRISPR/Cas9的優勢
①高效性:能夠在多種細胞類型和物種中實現高效的基因編輯,大大提高了基因編輯的成功率和效率,為大規模的基因功能研究和基因治療等應用提供了有力支持。
②簡便性:與傳統的基因編輯技術相比,CRISPR-Cas9 系統的構建和操作相對簡單。只需要設計和合成針對目標基因的 sgRNA,并將其與 Cas9 蛋白表達載體共同導入細胞中,即可實現基因編輯,無需復雜的蛋白質工程和基因克隆等操作,降低了實驗難度和成本。
③特異性:通過合理設計 sgRNA,可以實現對基因組中特定目標基因的精確編輯,具有較高的靶向特異性。同時,隨著技術的不斷發展和優化,對脫靶效應的控制也越來越有效,進一步提高了編輯的準確性和可靠性。
④多重編輯能力:可以同時設計多個針對不同靶位點的 sgRNA,實現對多個基因或同一基因的多個位點進行同時編輯,能夠更全面地研究基因之間的相互作用和復雜的生物學過程。
(五)CRISPR/Cas9的局限性
①脫靶效應:盡管經過不斷優化,CRISPR-Cas9 系統仍然存在一定程度的脫靶風險,即可能會在非目標位點產生切割和編輯,導致意想不到的基因突變,從而影響實驗結果的準確性和可靠性,甚至可能產生潛在的安全隱患。
②編輯效率問題:在某些細胞類型或特定的基因組區域,CRISPR-Cas9 的編輯效率可能不夠理想,無法達到預期的編輯效果,需要進一步優化實驗條件或采用其他輔助手段來提高編輯效率。
③PAM 序列限制:Cas9 蛋白識別的 PAM 序列相對有限,這在一定程度上限制了可編輯的靶點范圍。對于一些缺乏合適 PAM 序列的基因區域,可能無法直接使用常規的 CRISPR-Cas9 系統進行編輯,需要開發具有不同 PAM 特異性的 Cas9 變體或其他基因編輯工具來解決。
④倫理和法律問題:隨著 CRISPR-Cas9 技術在人類基因編輯等領域的應用逐漸深入,引發了一系列倫理和法律方面的爭議和擔憂,如生殖細胞基因編輯可能帶來的遺傳改變和倫理風險等,我們需要在技術發展的過程中建立健全相應的倫理準則和法律法規來規范其應用。

