

原代細胞應用指南——藥物篩選與疾病模型構建核心技術解析
 2025-06-13 16:17:10
2025-06-13 16:17:10
來源/作者:普拉特澤-生物醫學整體課題外包平臺
今天普拉特澤生物跟大家一起學習的是原代細胞實驗的常見問題—應用指南,高達70%的研究因細胞純度不足、傳代變異或功能丟失而失敗。
而普拉特澤生物——細胞檢測平臺也非常重視這一點,為廣大科研人員提供原代細胞實驗外包服務
同時也總結了在原代細胞實驗過程中常遇到的各種問題,分享給大家一起共勉!
效率與穩定性雙提升
1. 高活性細胞分離技術
▲防凋亡關鍵操作:
解離全程使用預冷無鈣鎂PBS,添加ROCK抑制劑Y-27632(10μM)阻斷失巢凋亡;
組織離體后4-6小時內處理,膠原酶濃度嚴格控制在0.1-0.3mg/mL,輔以DNA酶Ⅰ(100-300U)防止DNA粘稠物包裹細胞。
▲雜質清除策略:
□紅細胞污染:ACK裂解液處理2分鐘,離心清除;
□成纖維細胞污染:差速貼壁法(接種30分鐘移除非貼壁細胞)聯合免疫磁珠陰性篩選(抗Fibroblast微珠)。
2. 細胞轉染技術革新
▲智能自組裝核酸遞送:利用液-液相分離(LLPS)機制,在體外形成穩定核酸-蛋白納米顆粒;
▲高效低毒:人原代T細胞轉染效率達85%,且不影響CD34+造血干細胞分化潛能;
▲操作簡化:20分鐘完成GPCR激活檢測,僅需2μL樣本量。
從傳統藥篩到精準醫療
1. 高通量篩選平臺構建
●GPCR靶向藥篩模型:
瑞士ArcoScreen平臺采用微流控384孔板,直接對患者原代細胞進行非放射性篩選,可同步檢測Gα亞基偶聯作用,使II期臨床試驗失敗率降低50%;
操作流程:原代細胞+待測化合物 → 滴入試劑 → 熒光讀數(20分鐘出結果)。
2.高內涵成像應用:
威斯騰生物采用Operetta高內涵分析儀,實時監測藥物對細胞遷移、凋亡的多維度影響,適用于腫瘤干細胞靶向藥物篩選。
表1:三大藥物篩選平臺性能對比
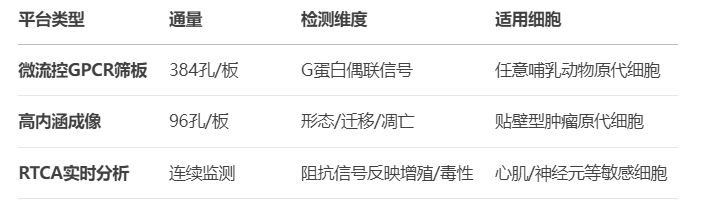
3. 腫瘤個體化治療模型案例
腎血管平滑肌脂肪瘤模型:
武漢賽爾朗靈團隊通過優化培養環境,實現原代細胞傳代10代不變異,STR鑒定為全球首例未記錄細胞系;
應用價值:基于患者原代細胞篩選mTOR抑制劑(如依維莫司),療效預測準確性提升40%。
3、疾病模型構建:從基礎研究到臨床轉化
1. 神經退行性疾病模型
原代神經元培養要點:
取材:新生鼠海馬組織(離體24小時內處理),0.125%胰酶消化15分鐘;
防膠質細胞增生:Neurobasal/B27無血清培養基 + Ara-C(終濃度10??mM)處理24小時;
功能驗證:誘導21天后檢測動作電位,Synaptophysin標記突觸形成。
2. 心血管疾病模型
血管平滑肌異常增殖模型:
分離技巧:小鼠主動脈中膜鈍性剝離,組織塊貼壁法培養(間距0.2-0.5cm),添加20%FBS的DMEM培養基;
表型維持:α-SMA免疫熒光鑒定,PDGF-BB誘導增殖模擬動脈粥樣硬化。
3. 罕見病研究模型
肺纖維化模型:
人原代肺成纖維細胞 + TGF-β1(10ng/mL)誘導,α-SMA表達上調提示肌成纖維細胞轉化;
藥物驗證:吡非尼酮抑制膠原分泌率>60%。
4.實操避坑指南:污染控制與表型維持
1. 污染防控六步法
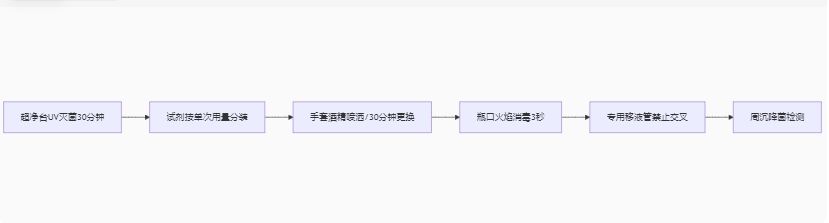
注:污染率可降至<1%3
2. 細胞老化的挽救策略
早期干預:
→傳代密度控制:貼壁細胞≥1×10? cells/cm2,避免過密導致接觸抑制;
→添加抗凋亡因子:Z-VAD-FMK(20μM)阻斷Caspase通路。
凍存規范:
凍存液配方:70%基礎培養基 + 20%FBS + 10%DMSO;
梯度降溫:4℃→-20℃→-80℃→液氮,復蘇時37℃水浴≤90秒。
5.、技術融合推動臨床轉化
類器官-原代細胞聯用模型:
肝癌原代細胞 + 肝星狀細胞共培養,構建3D類器官,模擬腫瘤微環境藥物抵抗;
AI驅動的藥效預測:
基于原代細胞轉錄組數據訓練神經網絡,提前預判藥物敏感性(如赫賽汀在HER2+乳腺癌模型中的響應準確率92%);
無血清培養基革新:
人源血小板生長因子(hPDGF)替代胎牛血清,降低批間差,滿足臨床級細胞生產需求。
原代細胞的應用價值建立在三重技術基石之上:
→嚴格時效性(離體至接種≤6小時);
→精準微環境模擬(生長因子組合+基質包被);
→跨尺度功能驗證(從免疫表型到電生理活性)
要資質有資質
要經驗有經驗
要案例有案例
好,原代細胞應用指南就介紹到這里啦~
有關于原代細胞培養和分離的任何問題或實驗咨詢
找她↓↓↓

